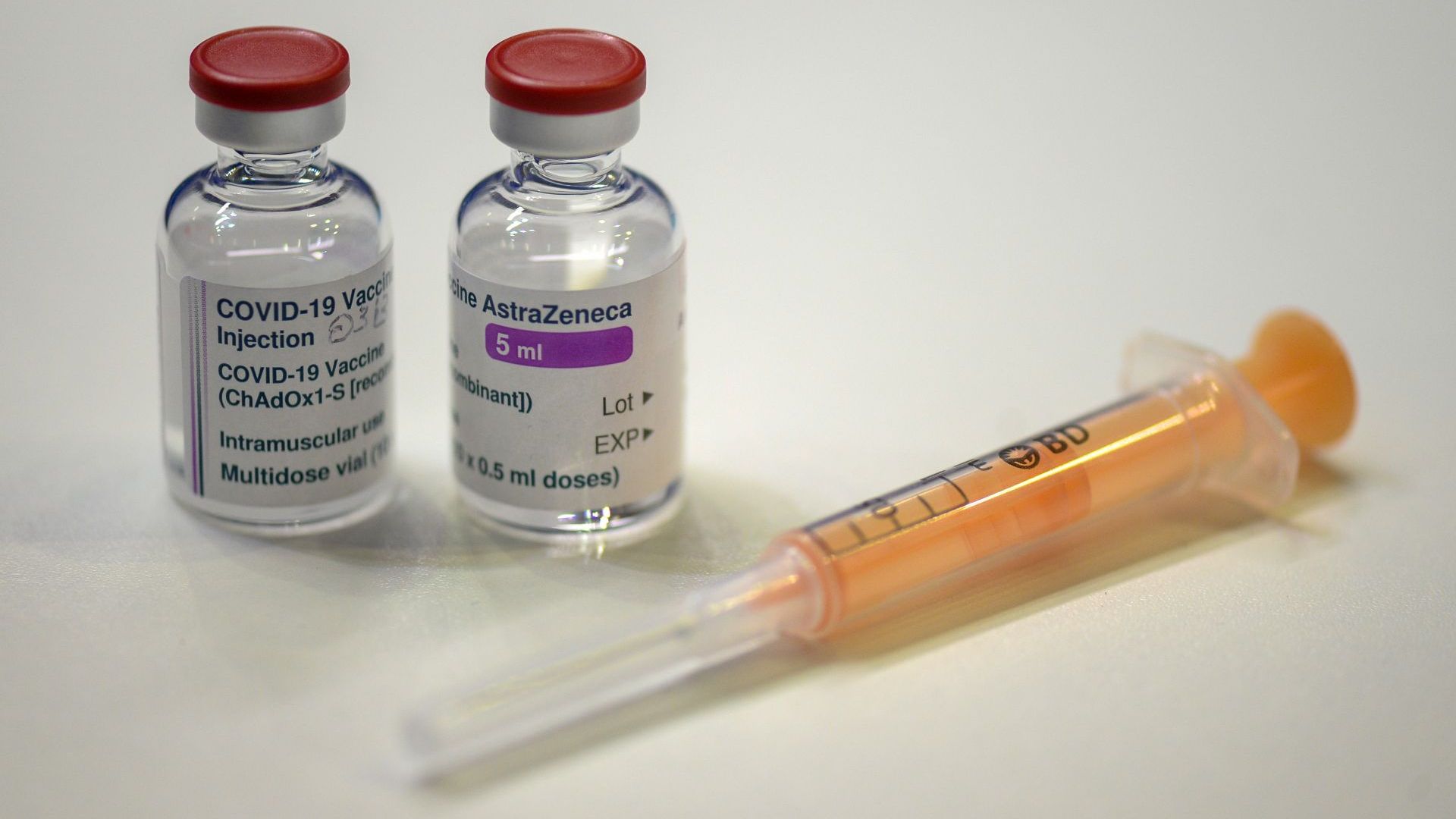
Европейската комисия съобщи, че издава пазарен достъп за ваксината на "АстраЗенека" - Оксфорд" срещу Ковид-19, одобрена по-рано днес и от Европейската агенция по лекарствата.
Това е третата ваксина, одобрена в ЕС, след препаратите на "Пфайзер" и "Модерна". Комисията отбелязва, че сега очаква изпълнение на договора за доставка на до 400 милиона дози от третата ваксина до края на годината.
Тази седмица ЕК и "АстраЗенека" влязоха в открит спор за доставките на ваксината, след като производителят съобщи, че не е в състояние да осигури нужните количества.
Преди седмица от компанията съобщиха, че до края на март за ЕС ще бъдат осигурени едва 25 на сто от очакваните количества.
Какви са особеностите на ваксината
Лекарствената агенция поясни, че тази ваксина е ефикасна в 59,9 на сто от случаите, като предотвратява заболяване от Ковид-19 или поне допринася за леко протичане на болестта. Ваксината се препоръчва само за пълнолетни хора.
Според агенцията засега няма достатъчно данни за действието на този препарат при хора над 55-годишна възраст, затова може да се препоръча в тази възрастова група да бъде използвана друга ваксина. Отбелязва се, че при препарата на "АстраЗенека" алергичните реакции са много редки и могат да бъдат много тежки.
Засега агенцията не знае дали ваксината предотвратява пренасянето на вируса на болестта, дали въздейства на мутациите на вируса и колко дълго осигурява защита. От агенцията отбелязаха, че тази ваксина би улеснила имунизацията в Европа, защото се съхранява и пренася по-лесно и това може да допринесе за ускоряване на европейската имунизационна кампания.
Агенцията по лекарствата препоръчва тази ваксина да се поставя на две дози, през четири до 12 седмици. Специалистите поясниха, че ваксината е подходяща и за преболедували Ковид-19.
Какво е планирано да получи България
От аденовирусната ваксина на "АстраЗенека - Оксфорд" България е заявила 4 518 232 дози при прилагането на две дози.